Еще один препарат для лечения СМА, Онасемноген абепарвовек (Золгенсма), в настоящее время одобрен Министерством здравоохранения РФ. Он вводится путем однократной внутривенной инъекции и имеет ограничения по возрасту и весу, но также используется для лечения маленьких детей.
«2,5 миллиона долларов за укол? Это реально столько стоит?»: почему лекарства от СМА такие дорогие
31 мая семье Гепаловых из Санкт-Петербурга удалось собрать 160 миллионов рублей с помощью своей общины, чтобы ввести двухлетнему Косте препарат для лечения спинальной мышечной атрофии (СМА). Вместе с Ольгой Германенко, руководителем фонда SMA Families Foundation, мы решили выяснить, что это за болезнь, почему лекарства от SMA такие дорогие и как мы можем помочь детям, живущим с этим диагнозом.
Спинальная мышечная атрофия (СМА) — это нервно-мышечное заболевание, при котором повреждение нервов приводит к прогрессирующей мышечной слабости. Он вызывается генетической мутацией в гене фактора выживания моторных нейронов (SMN1). В норме этот ген производит белок, который необходим для функционирования нервов, управляющих мышцами. У людей со СМА, страдающих мутацией в гене SMN1, этот белок вырабатывается в недостаточном количестве. В результате нервные клетки нарушаются и постепенно отмирают. Это приводит к сильной мышечной слабости, которая иногда приводит к летальному исходу. Прогноз заболевания зависит от типа СМА. В целом, чем раньше появляются симптомы, тем менее благоприятен прогноз.

Примерная частота встречаемости СМА составляет 1 на 11 000 новорожденных. Существует четыре основных типа СМА (типы I, II, III и IV). Тип СМА зависит от возраста, в котором появляются первые симптомы, и от тяжести мышечной слабости. Основным симптомом СМА является прогрессирующая мышечная слабость. По мере прогрессирования заболевания люди с СМА испытывают трудности с основными жизненными функциями — движением, дыханием и глотанием.
Однако СМА не влияет на способность человека думать, учиться или строить отношения с другими людьми.
При ЦМВ типа I рано поражаются мышцы, помогающие глотать и дышать, поэтому без лечения две трети пациентов умирают в течение первых двух лет жизни. При AMI II типа пациенты могут жить в подростковом и взрослом возрасте. При СМА III типа продолжительность жизни практически нормальная.
«СМА — это чрезвычайно серьезное наследственное нервно-мышечное заболевание, которое, если его не лечить, приводит к инвалидности, прогрессирует и угрожает жизни. Заболевание классифицируется как редкое (сиротское) заболевание. Долгое время для этой группы пациентов не существовало никакого лечения, и пациенты лечились только симптоматически. Однако в последние годы благодаря достижениям науки и медицины появились некоторые препараты, которые лечат причину заболевания», — объясняет Ольга Германенко, директор Фонда СМА.
Какое лечение от СМА существует сейчас
Полного и эффективного лекарства от СМА не существует. Лечение заболевания зависит от типа заболевания и симптомов, связанных с ним. В настоящее время в мире существует несколько препаратов, одобренных для лечения СМА. В основном это препараты, стимулирующие выработку белка SMN. К ним относятся нусинерсен (Spinraza) для детей и взрослых без ограничений по возрасту и типу, и ризиплам (Eurisdee) для взрослых и детей старше двух месяцев.
Кроме того, существует генная заместительная терапия. Препарат под названием Onasemnogen abeparvovec (Zolgensma), вводимый путем однократной внутривенной инъекции, одобрен для детей в возрасте до двух лет. Это лечение заменяет функцию дефектного гена SMN1. Стоимость введения препарата составляет около 2,5 млн. долл.

Почему этот препарат такой дорогой
Производимый компанией Novartis, препарат Золгенсма, безусловно, является самым дорогим лекарством в мире. Первая причина столь высокой цены — способность препарата «кардинально изменить жизнь семей, пострадавших от этого разрушительного заболевания». Вторая — это стоимость вывода нового препарата на рынок. При расчете стоимости будущего препарата обычно используется модель, учитывающая эффективность препарата и количество дополнительных лет жизни, которые будут иметь пациенты, получающие его. Таким образом, фармацевтические компании должны быть уверены, что они получат разумную прибыль на свои инвестиции и затраты на разработку.
В то же время, как бы абсурдно это ни казалось, препарат может быть экономически эффективным для пациентов: Для лечения требуется только одно введение препарата Золгенсма. В то же время один из альтернативных препаратов, Spinraza, используется пациентами несколько раз в год на протяжении всей жизни. Таким образом, «Спинраза» может стоить до 4 миллионов долларов в течение десяти лет. В настоящее время компания Novartis проводит лотерею, чтобы бесплатно выдавать препарат нескольким семьям в год. В 2020 году 170 детей во всем мире получили Золгенсму таким образом.
Что такое спинальная мышечная атрофия?
Спинальная мышечная атрофия (СМА) — это редкое генетическое заболевание, вызванное мутацией в гене SMN1 (выживающий моторный нейрон 1). Дефицит белка, кодируемого этим геном, приводит к дисфункции и гибели двигательных нейронов в стволе головного и спинного мозга. Поскольку двигательные нейроны контролируют работу мышц, у детей с СМА I типа (начало симптомов в возрасте 0-6 месяцев) развивается мышечная слабость и истощение, паралич развивается в среднем к 6 месяцам, и они умирают от дыхательной недостаточности к 2 годам.
Существуют различные типы СМА, в зависимости от тяжести заболевания. СМА I типа (около 50% случаев) возникает в первые месяцы жизни. СМА II-IV типа возникает позже в жизни и протекает несколько мягче. В дополнение к гену SMN1 у большинства людей также имеется ген SMN2. SMN2 имеет копию SMN1 в некоторых своих продуктах, но большинство из них дисфункциональны. Если у человека имеется более одной копии гена SMN2, тяжесть СМА обычно более легкая, но не всегда.
По данным Семейного регистра пациентов с СМА, в России насчитывается более 900 пациентов с СМА, но если экстраполировать данные из других стран, то их должно быть около 2500 — 3500, что означает недодиагностику в популяции. Ситуация изменится с внедрением пренатального скрининга и генетической диагностики.
Что такое Золгенсма?
Золгенсма — это генная терапия для лечения спинальной мышечной атрофии (СМА) с мутациями в обоих аллелях (варианты матери и отца) гена SMN1 (94% пациентов со СМА). В США препарат одобрен для пациентов в возрасте до двух лет. Это нормальная копия гена SMN1, встроенная в геном определенного вируса (адено-ассоциированного вируса серотипа 9, AAV9).
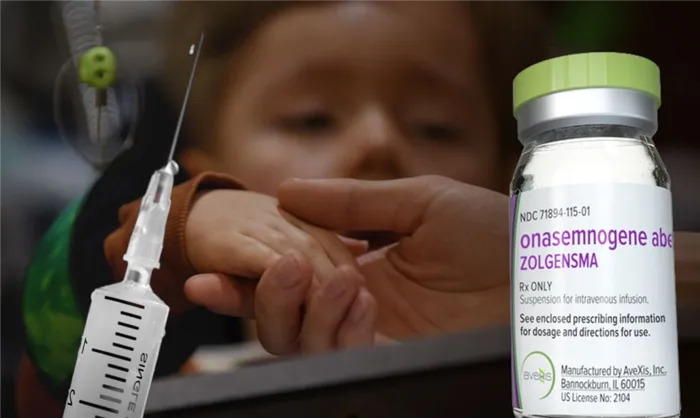
Препарат вводится пациенту однократно внутривенно. AAV9 хорошо проникает в клетки многих органов и тканей, включая двигательные нейроны, наиболее пораженные при СМА. Вирусная ДНК почти никогда не встраивается в геном клетки, а находится в виде одной молекулы в ядре, что повышает безопасность лечения с точки зрения генотоксичности. Клетки начинают вырабатывать нормальный белок SMN1, что должно благоприятно сказаться на течении болезни.
Какое лечение существовало до появления Золгенсмы?
До одобрения препарата Zolgensma единственным лекарством, направленным на причину заболевания, была Spinraza, которая была одобрена в США в конце 2016 года. Это относительно небольшая молекула, которая способствует производству полностью функционального белка SMN2. Таким образом, у пациентов с геном SMN2 вырабатывается белок, который удваивает функцию дефектного SMN1.
В клиническом испытании на детях в возрасте до двух лет, которое послужило основой для одобрения препарата, 61% детей остались живы и не зависели от непрерывной вентиляции легких (32% в контрольной группе). Улучшение двигательных навыков наблюдалось у 51% пациентов (и ни у одного из контрольной группы). У детей в возрасте 2-12 лет среднее улучшение после 15 месяцев лечения составило 3,9 балла по шкале моторных навыков, в то время как в контрольной группе среднее ухудшение составило 1 балл.
Наиболее распространенными нежелательными явлениями, связанными с приемом Spinraza, были респираторные инфекции и запоры. Также был отмечен повышенный риск тромбоцитопении, нарушений коагуляции и почечной токсичности.
В России препарат «Спинраза» был одобрен в начале 2019 года благодаря программе расширенного доступа компании Biogen, в рамках которой около 40 пациентов получают препарат бесплатно. Не все, кто нуждается в препарате, получают его.








